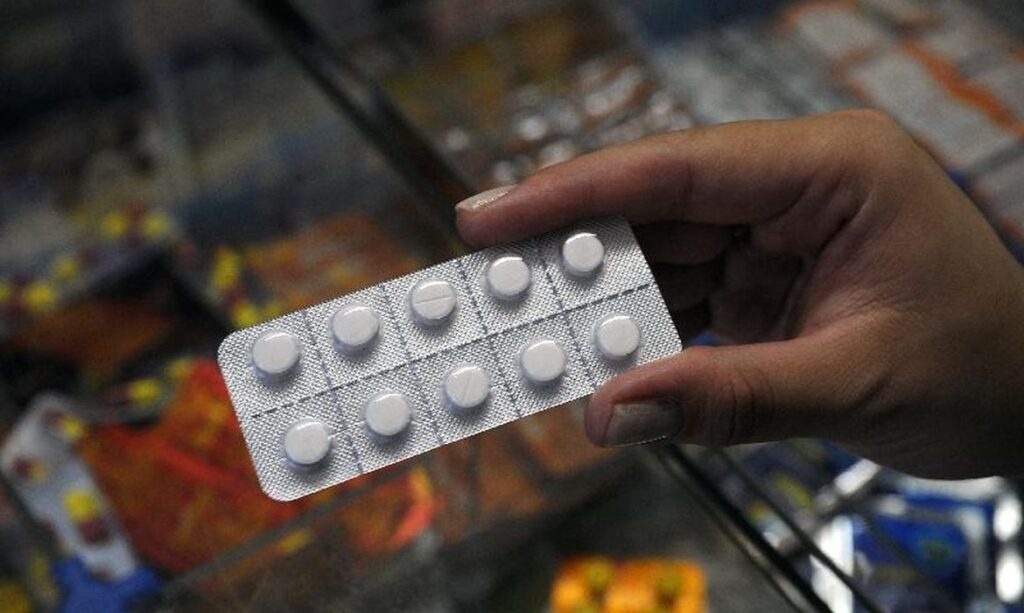
A Agência Nacional de Vigilância Sanitária (Anvisa) tomou uma medida crucial para a segurança dos consumidores nesta quarta-feira (8), ao determinar o recolhimento de um lote específico de dipirona monoidratada. O medicamento, na concentração de 500 mg/ml e apresentado em caixas com 100 ampolas de 2 ml de solução, é fabricado pela empresa Hypofarma. A decisão, que também inclui a suspensão da comercialização, distribuição e uso do produto, visa proteger a saúde pública diante da identificação de um sério desvio de qualidade.
A resolução da Anvisa, publicada no Diário Oficial da União, detalha que o lote afetado é o 24112378. A medida foi motivada pela confirmação da presença de material particulado não dissolvido, estranho à formulação original do medicamento. Esse tipo de contaminação representa um risco potencial à saúde dos pacientes, justificando a ação imediata do órgão regulador.
Material particulado: o desvio de qualidade e seus riscos
O cerne da questão reside na detecção de material particulado no lote da dipirona. Em produtos farmacêuticos injetáveis, como é o caso da solução em ampolas, a presença de partículas estranhas é considerada um grave desvio de qualidade. Essas partículas podem ser fibras, fragmentos de vidro, borracha, ou outras substâncias que não deveriam estar presentes na formulação.
A injeção de medicamentos contendo material particulado pode acarretar diversas complicações para o paciente. Entre os riscos estão reações inflamatórias no local da aplicação, formação de granulomas, obstrução de vasos sanguíneos e, em casos mais severos, embolia ou outras reações adversas sistêmicas. Por essa razão, a pureza e a integridade de medicamentos injetáveis são rigorosamente controladas pelas agências reguladoras, como a Anvisa, para garantir a segurança e eficácia do tratamento.
Suspensão imediata: o que muda para o mercado e pacientes
A determinação da Anvisa tem um impacto direto e imediato em toda a cadeia de distribuição do medicamento. A suspensão da comercialização significa que farmácias, hospitais e outros estabelecimentos de saúde não podem mais vender ou disponibilizar o lote 24112378 da dipirona da Hypofarma. A proibição de distribuição impede que o produto chegue a novos pontos de venda, enquanto a ordem de recolhimento exige que os estoques existentes sejam retirados do mercado.
Para os consumidores, a orientação é clara: caso possuam o medicamento do lote específico, devem suspender seu uso e procurar orientação médica ou farmacêutica. É fundamental que os pacientes verifiquem o número do lote em suas embalagens antes de qualquer uso. A agilidade na identificação e retirada desses produtos é essencial para minimizar qualquer risco à saúde pública.
O papel da Anvisa na garantia da segurança farmacêutica
A ação da Anvisa reforça seu papel fundamental na proteção da saúde dos brasileiros. Como órgão regulador, a agência é responsável por fiscalizar e controlar a produção, comercialização e uso de medicamentos no país. Desvios de qualidade, como o detectado neste caso, são frequentemente identificados por meio de monitoramento pós-comercialização, denúncias ou inspeções rotineiras.
A capacidade da Anvisa de agir rapidamente em situações como esta é um pilar para a confiança no sistema de saúde e na qualidade dos produtos farmacêuticos disponíveis. A transparência na divulgação dessas informações, por meio de publicações no Diário Oficial e comunicados à imprensa, é vital para que a população e os profissionais de saúde estejam cientes dos riscos e possam tomar as medidas adequadas. A Agência Brasil informou que entrou em contato com a Hypofarma e aguarda um posicionamento da empresa sobre o ocorrido, o que é um procedimento padrão em casos de recolhimento para que a fabricante possa esclarecer as causas e as ações corretivas.
Fonte: agenciabrasil.ebc.com.br